
中大新闻网讯(通讯员赵萌)目前,面对血液恶性肿瘤、再生障碍性贫血和地中海贫血等骨髓衰竭性疾病,造血干细胞移植(HSCT)已被证实是有效的治疗手段,也是核辐射损伤的唯一治疗手段。这是因为干细胞具有极强的长期自我更新及多项分化潜能,但仍有5-20%的患者会发生原发或继发性造血干细胞植入不良,影响最终的治疗效果。因此,研究导致植入不良的主要机制将有助于进一步提高治疗成效。
近日,中山大学中山医学院赵萌教授和孙逸仙纪念医院蒋琳加研究员联合带领的团队在Blood期刊上发表了文章“The RIG-I-NRF2 axis regulates the mesenchymal stromal niche for bone marrow transplantation”,研究论文揭示了骨髓间充质干细胞(MSC)调控造血干细胞移植的新机制。
此前研究表明,骨髓微环境损伤是导致植入不良的主要机制之一。间充质干细胞作为骨髓微环境的重要细胞组成,是具有成骨、成脂肪和成软骨分化能力的成体干细胞,同时,还具有支持造血干细胞的功能。因此,间充质干细胞被广泛应用于临床细胞治疗。
赵萌教授团队认为探讨间充质干细胞调控造血干细胞植入不良的机制,具有重要的基础和临床意义。临床研究发现,药物处理、感染和炎症反应等刺激因素与造血干细胞植入不良密切相关,然而这些刺激因素导致骨髓微环境损伤进而影响造血干细胞植入不良的机制还不清楚。
赵萌教授研究团队系统研究了RIG-I-NRF2信号通路对骨髓间充质干细胞成骨分化和支持造血重建功能的调控作用和分子机制,并进一步证实骨髓间充质干细胞的RIG-I-NRF2信号是调控造血干细胞移植后应急髓系分化(Emergency myelopoiesis)抵抗细菌感染的关键机制。
RIG-I维甲酸诱导基因-I(retinoic acid-inducible gene I)最初是在维甲酸(ATRA)诱导白血病分化治疗研究中发现的维甲酸上调基因。此次研究发现,维甲酸、干扰素、细菌感染等刺激可以在间充质干细胞中显著上调RIG-I基因的表达,导致间充质干细胞的成骨分化能力受损,从而诱发骨质疏松症,并且还会损伤间充质干细胞的造血支持功能,进而导致造血干细胞移植后的植入不良和移植后的细菌感染等并发症。
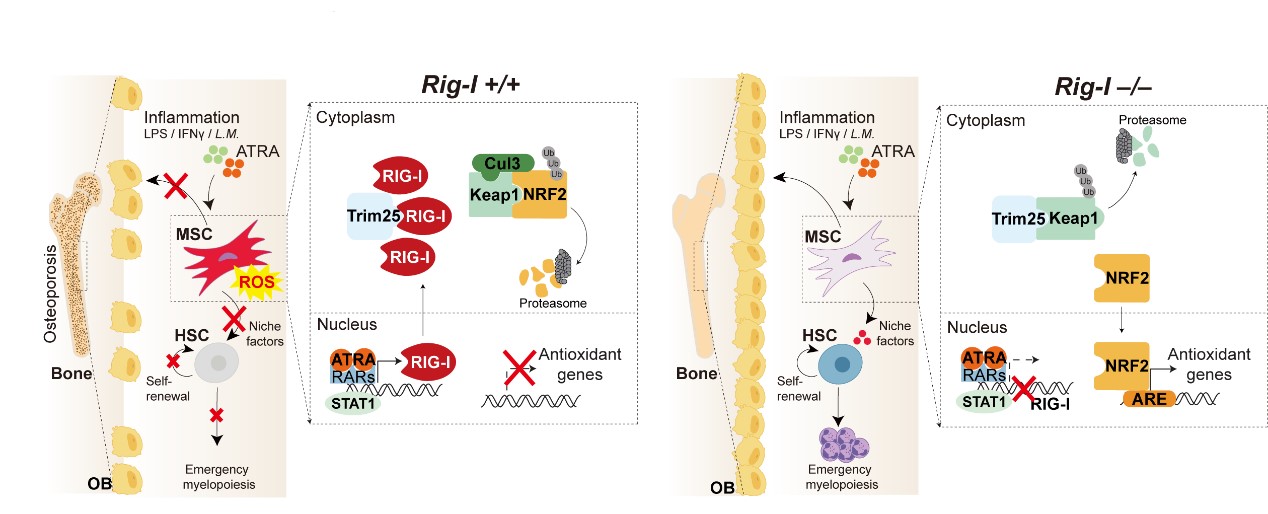
骨髓间充质干细胞RIG-I-NRF2通路调控造血干细胞移植
研究还证实,RIG-I通过降解细胞抗过氧化分子NRF2导致细胞过氧化物增加是损伤间充质干细胞的关键。此发现与移植后患者的临床转化研究相一致,提示对骨髓微环境的抗氧化干预是治疗移植后植入不良和细菌感染等并发症的有效手段,能够有效缓解在药物和感染刺激条件下因MSC损伤所导致的骨质疏松症和造血、免疫功能障碍。
此外,研究团队还发现恢复MSC的成骨分化能力并不能有效的恢复其造血支持能力,表明MSC成骨分化和造血支持可能是由不同功能亚群介导,因此进一步解析MSC参与成骨分化和造血支持不同功能亚群的调控机制和制备策略,将为开发针对不同适应症的MSC细胞治疗药物奠定基础。
赵萌教授和蒋琳加研究员为本文的共同通讯作者,娄琪博士后、蒋凯证硕士研究生和许泉辉八年制博士研究生为本文的共同第一作者。本项目得到了基金委优秀青年基金、干细胞重点研发项目和中山大学中山医学院-附属第一医院先进医学科学技术研究中心的支持。