
中大新闻网讯(通讯员赵现廷)10月1日,中山大学肿瘤防治中心徐瑞华教授团队领衔的一项1b期临床研究(NCT05890742)发表于国际顶级期刊Cancer Cell。研究采用前瞻性随机对照设计,系统评估了信达生物伊匹木单抗N01(IBI310)联合信迪利单抗对比PD-1单药,在局部进展期微卫星高度不稳定/错配修复缺陷(MSI-H/dMMR)结肠癌新辅助治疗中的疗效与安全性。首次以高水平的循证证据验证中国双免方案可显著提高病理完全缓解率(pCR)达78.4%,在中位随访21.4个月内无患者复发,安全耐受,为优化该类患者的新辅助治疗模式提供了有力支持。

研究以封面文章发表于Cancer Cell
封面展示的是黄河与洮河的交界处,它位于甘肃省临夏回族自治州永靖县境内,两河于此相拥——浑浊湍急的洮河携着黄土高原的赭黄,与湛清缓流的黄河水相遇,形成一道“半江碧水半江浑”的天然奇观。正如我们Neoshot IB临床研究中CTLA4抗体IBI310(洮河)如烈马奔腾而下,注入PD-1抗体信迪利单抗(黄河)的怀抱,二者碰撞交融,泾渭分明却又最终合一,最终将黄河渲染成大地的血脉。犹如历史长河在此刻定格——既是自然的磅礴诗篇,也是民族生生不息的隐喻。
结直肠癌是全球第三大常见恶性肿瘤,也是癌症相关死亡的第二原因。约有15%的结直肠癌患者存在微卫星高度不稳定/错配修复缺陷(MSI-H/dMMR),该类肿瘤因其高突变负荷,产生大量新抗原,使得肿瘤微环境对免疫治疗更为敏感。既往针对局部晚期(Ⅱ-Ⅲ期)MSI-H/dMMR患者的治疗,尽管手术是核心治疗手段,但高危患者(如T4或N2)术后复发风险较高,而传统新辅助化疗对dMMR肿瘤疗效有限。近年来,免疫检查点抑制剂(ICIs)在转移性MSI-H/dMMR结直肠癌中展现出显著疗效,推动了其在局限性肿瘤新辅助治疗中的探索。然而,ICIs在新辅助治疗中的价值,尤其是双免疫联合方案能否较单药带来更好的获益,目前相关数据较为有限。
本研究是一项随机对照、开放标签、多中心1b期临床试验(NCT05890742),研究共纳入101名局部晚期可切除MSI-H/dMMR结肠癌患者,随机分配双免疫方案组(n=52),接受伊匹木单抗N01注射液(IBI310)+信迪利单抗治疗,共2个治疗周期;或单药组(n=49),接受信迪利单抗单药治疗。新辅助治疗后进行手术评估。主要终点为改良意向治疗人群(mITT)(接受至少一次新辅助治疗且完成手术)的pCR率,次要终点包括无事件生存期(EFS)、总生存期(OS)、R0切除率和安全性。
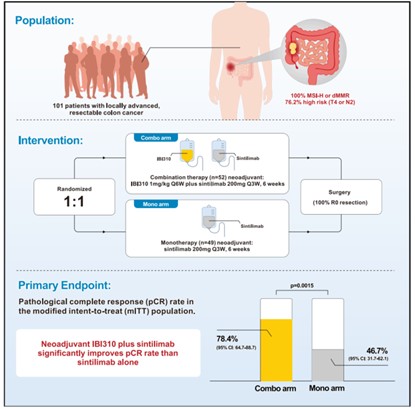
研究方案设计
病理完全缓解率达78.4%,中国双免方案创造新纪录
mITT中,双免疫方案组病理完全缓解率(pCR)率高达78.4%,显著高于单药组的46.7%,组间差异为28.3%(95% CI: 10.8-45.7, p=0.0015)。意向治疗人群(ITT)和符合方案人群(PP)亦得出一致结果,分别为76.9%和80%,均支持联合用药显著提高pCR。
与既往研究中ICIs单药新辅助治疗的pCR率59%–65%及双免疫联合治疗的pCR率60%–68%相比,均实现大幅提升,刷新历史记录,为结肠癌新辅助免疫治疗领域带来全新突破。
此外,双免疫方案组主要病理缓解率(MPR)率也高达94.1%(残留活肿瘤细胞RVT ≤10%),优于单药组73.3%,与NICHE-2研究(MPR 95%)和NICHE-3研究(MPR 92%)结果相当,这一结果足以反映出中国双免方案优于PD-1单药治疗的临床获益。
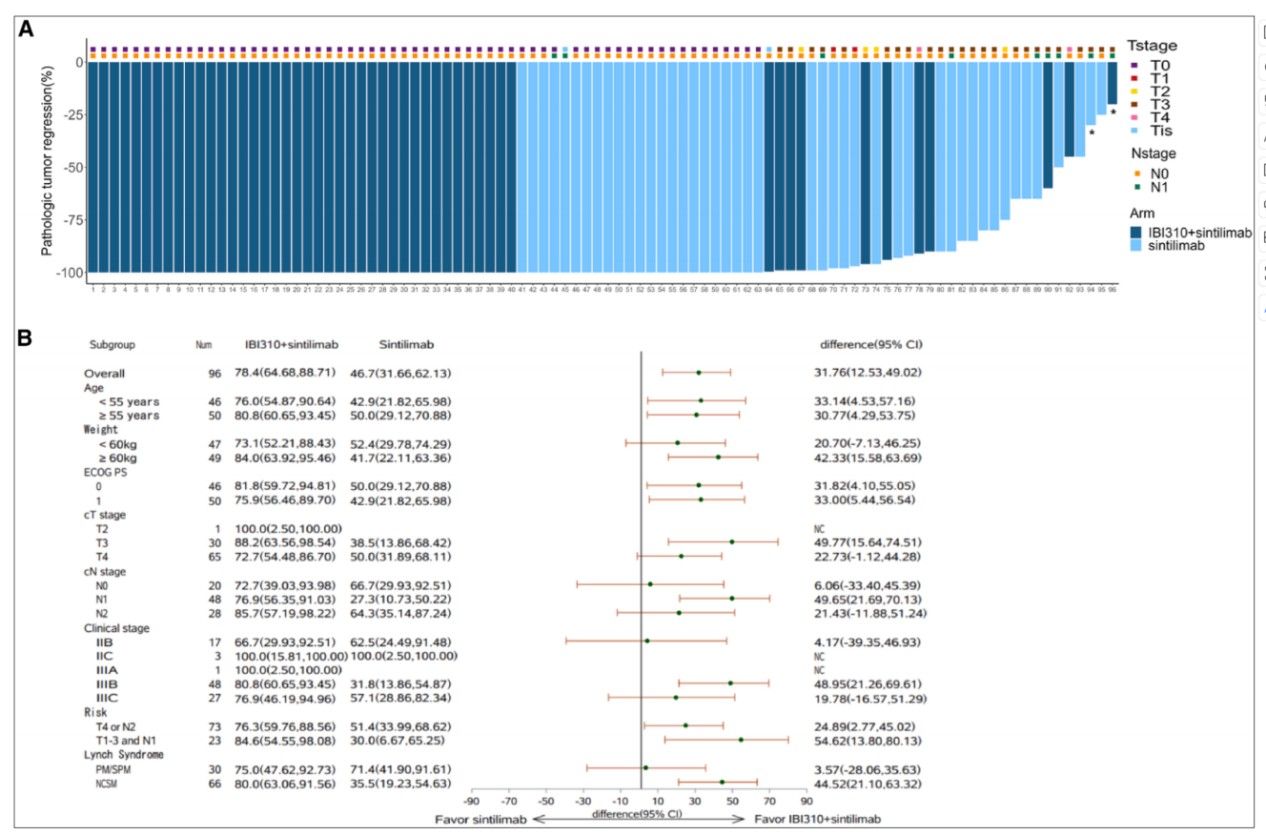
主要终点病理完全缓解率
在分层亚组分析中,研究进一步揭示了不同遗传背景及临床分型对疗效的影响。非林奇综合征相关突变患者中,双免疫方案组的pCR率高达80.0%,远高于单药组的35.5%,组间差异36.7%(95% CI: 16.7-56.7)。而携带林奇综合征致病性/或疑似致病性突变患者,两组pCR率均超过70%,差异不显著。
所有患者实现R0切除,21.4个月中位随访期内无复发
接受标准治疗(包括手术和辅助治疗)的局部晚期dMMR结肠癌患者实现R0切除挑战大且复发率风险较高。在本研究中,尽管76.2%的患者属于高危人群,但所有患者均成功实现R0切除,术后中位随访时间为21.4个月(范围:1.5-24.6),在随访期间未见疾病复发,意味着双免疫新辅助治疗可能大幅降低远期复发风险。目前,EFS与OS数据仍在持续随访中,其长期生存获益值得进一步期待。
安全可控,中国双免方案无新增风险
安全性方面,治疗相关不良事件(TRAEs)发生率在双免疫方案组为71.2%,单药组为49.0%;≥3级TRAEs发生率分别为3.8%和10.2%。多数TRAEs为1-2级,提示两种治疗方案均具有良好耐受性,且联合用药未显著增加严重不良事件风险。
免疫相关不良事件(irAEs)发生率在双免疫方案组为48.1%,单药组为38.8%。≥3级irAEs发生率分别为3.8%(包括免疫性心肌炎和肠炎)和8.2%(包括免疫性心肌炎、皮疹、甲状腺功能减退和丙氨酸氨基转移酶升高)。手术期并发症及死亡率在两组中均无统计学差异,未出现新的安全信号。
此外,一项随机对照、多中心Ⅲ期临床试验(NeoShot-III研究,NCT05890742)正在进行中,将进一步验证双免疫治疗方案与术后辅助化疗在MSI-H/dMMR结肠癌患者中的疗效与安全性,为其成为MSI-H/dMMR结肠癌新辅助治疗方案提供更充分的循证证据支持。
作为随机对照用于MSI-H/dMMR结肠癌新辅助治疗的临床研究,试验采用的伊匹木单抗N01(IBI310)与信迪利单抗均为我国自主研发的原研药物。本研究成功发表于国际顶刊Cancer Cell,是中国肿瘤临床研究创新迈向世界前沿的有力印证。“中国双免方案”凝聚中国智慧,立足中国需求,更展现了服务全球患者的潜力。我们期待这一中国方案能尽快落地临床,为结肠癌治疗领域带来变革,惠及更多患者。
论文链接:
https://www.cell.com/cancer-cell/fulltext/S1535-6108(25)00396-4