
我校药学院罗海彬教授研究团队自主发展了加速的自由能微扰-绝对结合自由能计算新方法(GA-FEP),取得药物设计关键技术的新突破,实现自由能微扰(FEP)/药物设计方法的国产化和自主可控。在抗击新冠肺炎研究中,该GA-FEP方法首次一周内完成对老药数据库的高精度筛选,从而预测出25个对新冠肺炎主蛋白酶Mpro有较高亲合力的药物,进一步的体外活性验证发现了15个Mpro抑制剂(Ki 为 0.04至3.3 µM),表现出较高的活性化合物命中率。特别值得一提的是,抑制活性最优的药物双嘧达莫对新冠肺炎获得较好的临床治疗效果,从而进一步验证GA-FEP方法的可靠性。该GA-FEP方法既可以明显提高药物/靶标亲合力的预测精度(理论亲合力与实验亲合力差值绝大多数小于2 kcal/mol),还可以提高预测速度(传统FEP方法每个化合物的预测时间为30-60天,本方法缩短为1天以内,效率提高30-60倍),从而提高创新药物筛选的成功率并降低研发时间。除了高精度筛选外,该GA-FEP方法还可以应用于其他新药设计工作中,如骨架跃迁和全新药物设计等,以提高先导化合物的发现和优化效率。
上述研究结果,于2020年10月13日以Article形式发表在PNAS,题为"Identify potent SARS-CoV-2 main protease inhibitors via accelerated free energy perturbation-based virtual screening of existing drugs"。中山大学药学院李哲博士、中国海洋大学医药学院李昕博士生和中山大学药学院黄仪有博士为本文的并列第一作者。本文通讯作者为中山大学药学院罗海彬教授、中国海洋大学医药学院王鑫教授、肯塔基大学药学院湛昌国教授和中山大学生命科学学院崔隽教授。中科院上海药物所、兰州大学、广州医科大学等单位也参与本课题的研究。
本研究得到了国家重点研发计划、国家自然科学基金优秀青年基金等经费的支持,同时也得到了腾讯云,广州、深圳、天津、北京等超级计算中心的大力支持。
研究背景:
当前人类健康领域面临若干的重大挑战,包括重大疾病(如恶性肿瘤、糖尿病、心血管疾病等)及突发的恶性传染病(如新冠肺炎、SARS、埃博拉等)。因此,亟需加快新药研发速度,以应对以上挑战,尤其是大规模突发疫情来袭之时,尽快获得应急药物以控制疫情的发展。如何精准预测药物与靶标的亲合力(结合自由能)以获得高亲合力的小分子药物,一直是计算机辅助药物设计领域的“圣杯”,若能精准预测药物/靶标亲合力,将能加速先导化合物药物的发现及优化效率,从而明显缩短新药创制周期及降低研发成本。
自由能微扰(FEP)是一种基于统计力学理论严格推导而来的方法,具有较高的理论精度,在药物/靶标亲合力预测方面具有很好的应用前景。然而,该类方法对计算资源消耗极大(传统CPU服务器使用该方法预测一个药物与靶标亲合力需要1-2个月),且缺乏公认的最佳流程,尚未得到广泛的应用。近年,药物设计顶级软件薛定谔发展的自由能微扰/相对自由能预测方法受到制药和科研工作者的极大关注(JACS 2015, 137, 2695),然而该方法主要被应用于预测结构相似配体间的相对结合自由能(一般两配体结构差异小于10个重原子),无法预测不同骨架的化合物与靶标的亲合力,且许可费用昂贵,限制了该方法的应用范围。
本次进展:
1.发展了自由能微扰新方法GA-FEP,取得药物设计关键技术的新突破,实现自主可控
药学院罗海彬/李哲研究团队一直致力于将现代物理学手段应用于新药研发,以提升药物/靶标亲合力的预测精度及速度。为了发展基于FEP的新方法,并推动该方法真正应用于新药设计,该项目团队发展了基于FEP的绝对结合自由能计算方法(GA-FEP)。前期工作中,他们通过研究FEP计算得到的概率分布特征,研发了第一代用于预测药物/靶标亲合力(绝对结合自由能)GA-FEP方法,并成功将该方法应用于PDE10抑制剂先导化合物的设计和结构优化(从苗头化合物到先导化合物,抑制活性得到了2000多倍的提升,J. Med. Chem. 2019, 62, 2099–2111)。
为了大幅度提高GA-FEP的预测速度,以提高药物设计效率,项目组推导了能准确描述FEP热力学循环中添加束缚步骤 概率分布的公式,并将其命名为RED函数。RED函数极大加速了GA-FEP方法的预测速度。如图1(a)所示,计算约束能量过程中,采样得到的 (黄点)可以很好地被RED函数拟合(红线)。通常来讲,约束能量需要12个λ窗口才能够准确计算。而经RED函数分析,拟合,并计算能量后,相比于通常的12个λ窗口,新方法使用一步微扰(2个λ窗口)即可准确计算约束能量。使用3个靶标及28个配体进行测试,工作中发现一步微扰(2λ窗口)以及12λ窗口得出的结果基本一致,具有极好的相关性(如下图所示),对于所有体系,两种方式计算得到的误差小于0.5 kcal/mol。这些工作和发现极大加速了FEP-ABFE的预测速度,并使得GA-FEP方法首次能应用于新药的虚拟筛选研究中。
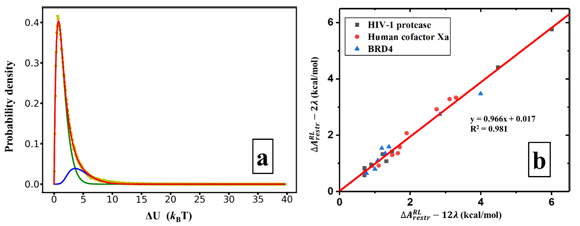
图1. RED函数明显加快预测速度
2.实现GA-FEP方法在突发疫情应急药物响应方面的典型应用
新冠病毒肺炎大流行已成为全球性危机,但目前尚缺少针对新冠肺炎的有效治疗方法。通过老药新用,有望快速发现较为安全的新冠肺炎治疗药物。团队采用了如图2所示的研究策略,从已知药物化合物库(含2500种药物)中寻找针对新冠肺炎的治疗药物。以新冠病毒SARS-CoV-2主蛋白酶(Mpro)为靶点,首先经过分子对接得到100个分子,而后一周内完成了该100个化合物与Mpro的GA-FEP预测,预测出25个老药分子,体外生物实验验证15个药物对Mpro具有较高的抑制活性(Ki均小于4 μM),活性药物的成功率高达60%。特别值得一提的是,这16个药物与靶标的理论亲合力与实验亲合力差值绝大多数均小于2 kcal/mol,而药物设计中常用的MM-PBSA和GBSA两种方法得到的差值均大于10 kcal/mol,充分说明GA-FEP方法在药物/靶标亲合力的预测精度方面具有明显的优势。总的来说,GA-FEP方法不但可以提高药物/靶标亲合力的预测精度,还可以明显提高预测速度(传统FEP方法每个化合物的预测需要30-60天,本方法缩短为1天以内,效率提高30-60倍),从而提高创新药物筛选的成功率并降低研发时间。
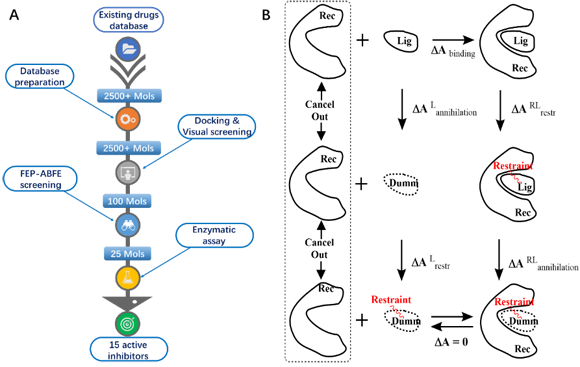
图2. 本研究采用基于GA-FEP的高精度筛选策略
有意思的是,坎地沙坦酯的代谢产物坎地沙坦也对Mpro具有较好的抑制活性。Disulfiram和Atazanavir在其他报道中也被确证为Mpro抑制剂,其余14个均由本文首次发现为Mpro抑制剂。16个药物中,抑制活性最高的化合物为由本方法首次发现的双嘧达莫(Dipyridamole,图3),Ki为40 nM,进一步病毒细胞实验获得该化合物的EC50 为100 nM。特别值得一提的是,在后续两轮多中心临床实验中,验证了该化合物具有较好的治疗效果:在超过100例的临床试验中,普通型新冠患者三周出院率为100%,重型患者三周出院率为87.5%。部分临床结果已发表在药学权威期刊Acta Pharm. Sin. B(2020, 10, 1205-1215),并入选今年7月份该刊的封面故事。
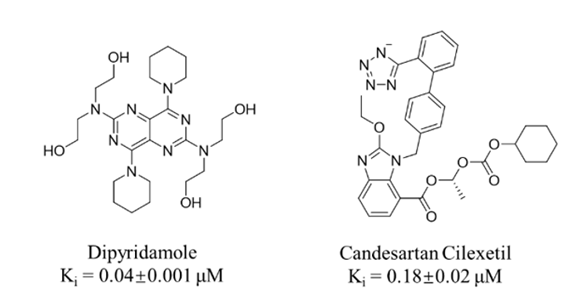
图3. 通过自由能微扰GA-FEP方法高精度筛选获得2个活性最优的Mpro抑制剂